STTT丨EB病毒劫持組蛋白去甲基化途徑促進上皮腫瘤惡性進展的新機制
EB病毒(Epstein-Barr virus, EBV)是首個被發現的人類腫瘤相關病毒,每年全球因EBV感染新發的腫瘤病例約20萬例。其中,源自上皮組織的惡性腫瘤——鼻咽癌(Nasopharyngeal carcinoma, NPC)和EBV相關胃癌(EBV-associated gastric cancer, EBVaGC)占比高達80%,嚴重威脅著人類的健康。儘管眾多研究已證明EBV與這些上皮惡性腫瘤的高度關聯,然而其驅動腫瘤發生和發展的致癌機制仍未被完全解析。
組蛋白修飾是表觀遺傳學的重要調控機制之一,包括甲基化、乙醯化、磷酸化和泛素化等多種修飾類型。研究表明,組蛋白修飾的變化在腫瘤的惡性進展中發揮關鍵作用,且靶向異常表達的組蛋白修飾因數已顯示出良好的抗腫瘤效果。已有研究揭示EBV感染可以影響上皮腫瘤宿主基因的組蛋白修飾的改變,然而其具體機制仍未明確。因此,鑒定EBV介導的相關上皮腫瘤中組蛋白修飾關鍵因數,並深入探討其作用機制,將有助於理解EBV致病機制,探索潛在的表觀遺傳治療靶點,從而為EBV相關上皮腫瘤的治療提供新策略,改善患者預後。
中山大學腫瘤防治中心研究員、中山大學香港高等研究院院長助理貝錦新團隊在Signal Transduction and Targeted Therapy期刊上發表了題為Epstein-Barr virus hijacks histone demethylase machinery to drive epithelial malignancy progression through KDM5B upregulation 的研究論文。該研究利用單細胞轉錄組、全轉錄組等多組學數據分析,鑒定了賴氨酸去甲基酶5B(Lysine demethylase 5B, KDM5B)為EBV相關上皮腫瘤惡性進展過程中的關鍵組蛋白修飾因數;進一步結合體內、體外模型和分子機制研究,揭示了EBV感染上調KDM5B表達促進上皮腫瘤惡性進展的作用機制,並探討了靶向KDM5B治療EBV相關上皮腫瘤的臨床應用前景。

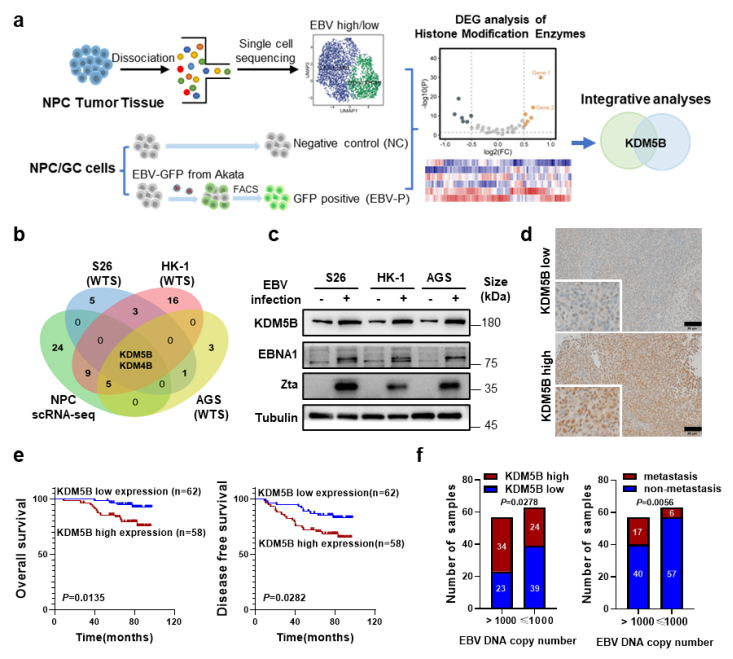
該研究採用多組學整合分析和體外EBV感染模型,聯合鼻咽癌組織單細胞測序數據、EBV陽性的鼻咽癌和胃癌細胞全轉錄組測序數據以及組蛋白修飾因數資料庫,鑒定KDM5B為EBV感染促進上皮腫瘤惡性進展過程中的關鍵組蛋白修飾因數(圖1a-c)。進一步臨床分析顯示,KDM5B高表達與鼻咽癌患者不良預後顯著相關,且其高表達與患者體內高EBV DNA水準密切相關(圖1d-f),提示了 KDM5B在 EBV 相關上皮腫瘤惡性進展中的重要作用。
該研究進一步揭示了EBV促進KDM5B表達的分子機制:EBV潛伏基因EBNA1與轉錄因數CEBPB結合形成複合物,協同促進KDM5B的轉錄,且該調控關係依賴於EBV的存在;EBV 即刻早期裂解階段中的關鍵分子BZLF1通過與KDM5B啟動子上的BZLF1結合元件(ZRE)直接結合促進KDM5B的轉錄,而該轉錄啟動作用可以獨立於EBV的存在。值得關注的是,EBNA1和BZLF1對KDM5B的作用位點相距僅 55bp,但二者對KDM5B的轉錄啟動作用是相互獨立的,這表明 EBV 可能策略性地調控這一關鍵區域,從而在整個潛伏-裂解生命週期中調控宿主基因組的組蛋白修飾。
為了探究EBV介導的KDM5B表達上調促進EBV相關上皮腫瘤惡性進展的作用機制,該研究對敲低KDM5B的EBV陽性鼻咽癌細胞HONE1-EBV進行了ChIP-seq和RNA-seq聯合分析;結合實驗驗證發現,PLK2 是受 KDM5B 調控最顯著的靶點,KDM5B 通過降低 PLK2 啟動子處的 H3K4me3水準抑制PLK2 轉錄。一系列回補實驗和臨床樣本免疫組化染色分析證實了KDM5B通過抑制PLK2表達從而促進EBV相關上皮腫瘤的惡性進展。同時,該研究利用EBV陽性鼻咽癌人源性腫瘤組織異種移植瘤模型(Patient-Derived Xenografts, PDX)和胃癌細胞系來源異種移植瘤模型(Cell-line Derived Xenograft, CDX),開展了靶向 KDM5B的抑制劑(AS-8351)治療 EBV 相關上皮腫瘤的臨床前研究。體內、體外實驗模型結果顯示,KDM5B 抑制劑處理顯著抑制了PI3K/AKT/mTOR信號通路,並明顯減緩了腫瘤的惡性進展。
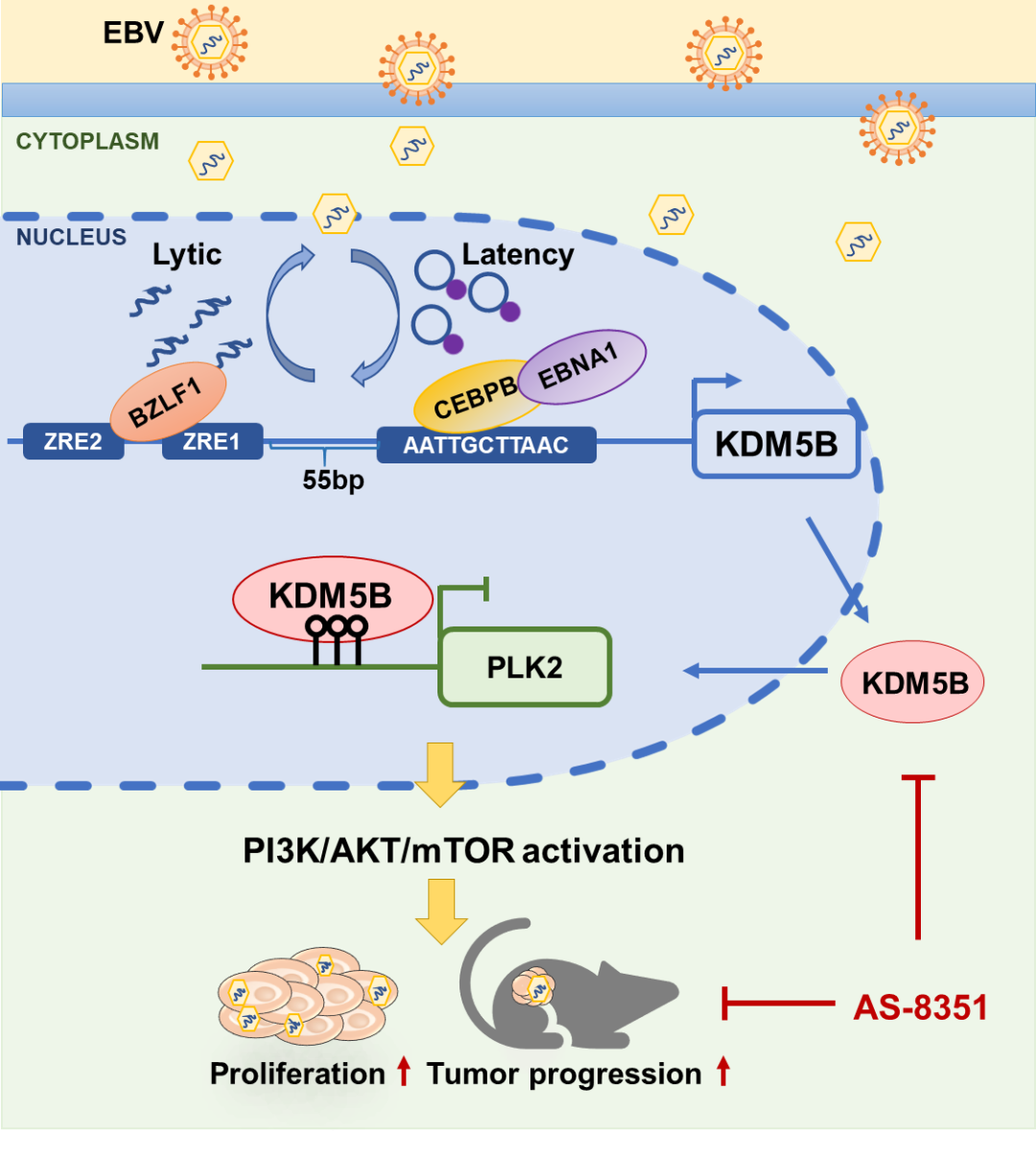
綜上,該研究發現EBV編碼的潛伏基因EBNA1與轉錄因數CEBPB結合促進KDM5B轉錄,而裂解基因BZLF1直接與KDM5B啟動子上的ZRE結合促進KDM5B轉錄;EBV介導的KDM5B上調進一步通過H3K4me3去甲基化途徑抑制PLK2的表達,從而啟動下游PI3K/AKT/mTOR信號通路,促進EBV相關上皮腫瘤的惡性進展;靶向KDM5B的抑制劑AS-8351可顯著抑制EBV相關上皮腫瘤的惡性進展(圖4)。該研究揭示了 EBV通過調用宿主基因組蛋白修飾途徑促進上皮腫瘤惡性進展的機制,並提出了靶向EBV、KDM5B及其下游調控網路來治療EBV相關上皮腫瘤的潛在策略。
中山大學腫瘤防治中心周雅青博士研究生(現為博士後)為該論文第一作者,中山大學腫瘤防治中心貝錦新研究員和羅春玲副研究員為該論文的共同通訊作者;香港大學關新元教授、新加坡國立癌症研究中心Choon Kiat Ong教授、澳門大學Vivien Ya-Fan Wang教授共同參與了本研究。
原文鏈接:https://www.nature.com/articles/s41392-025-02163-5貝錦新課題組主要從事精准醫學和轉化醫學研究,針對腫瘤臨床表徵異質性,利用個體和單細胞水準的基因組、表達譜等多層次、多組學資訊,挖掘與腫瘤發生發展及其異質性相關的分子、細胞及其作用網路,研究候選分子、細胞調控腫瘤進展的重要機制,發現與腫瘤早期精准診斷相關的分子標誌物,篩選針對腫瘤微環境演進關鍵事件的精准診治靶標,為實現腫瘤的個體化防診治提供有效解決方案。至今發表SCI論文110餘篇,其中包括國際頂級專業雜誌Cell、Lancet Oncology、Nature Genetics、Journal of Clinical Investigations, Nature Communications等。課題組長期招聘各類科研人員,歡迎對相關領域感興趣的博士後,博士生加入。

